【研究背景】
肝细胞移植是治疗终末期肝病的有效方法。然而,由于人类肝细胞的供应有限,猪肝细胞作为一种潜在的替代来源引起人们的广泛关注。尽管如此,传统的原代猪肝细胞在功能维持和体外增殖方面表现出一定的局限性。
【成果简介】
南方医科大学的高毅教授团队最近发表在《Biomedcine & Pharmacotherapy》的一篇文章“HDAC inhibitors support long-term expansion of porcine hepatocytes in vitro”通过使用组蛋白去乙酰化酶抑制剂(HDACi)将原代猪肝细胞去分化为具有高增殖潜力的肝祖细胞。这些肝祖细胞可以很容易分化成成熟的肝细胞,最终通过微胶囊化移植到患有急性肝衰竭的小鼠体内后,可显著提高其存活率。
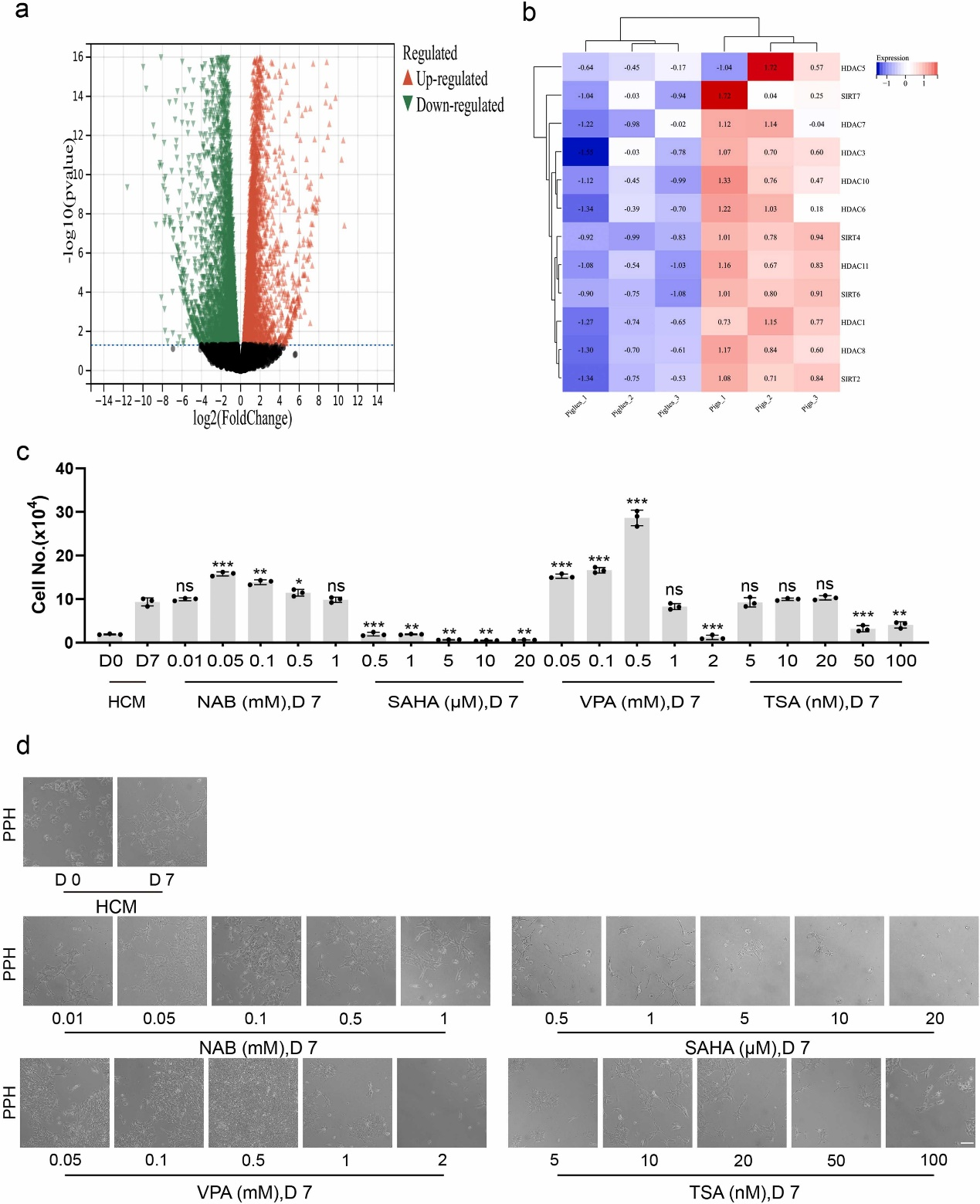
HDACi (VPA)促进原代猪肝细胞的体外扩增:作者将原代猪肝细胞分别在含有四种常用HDACi(NAB, SAHA, VPA和TSA)的经典肝细胞培养基(HCM)下培养7天,结果表明,含有0.5 mM VPA的HCM (简称:VPA-HCM)可显著促进原代猪细胞生长,其细胞数量约为同等纯HCM培养条件下数量的三倍(图1c和d)。
图1. HDACi促进原代猪肝细胞的体外扩增
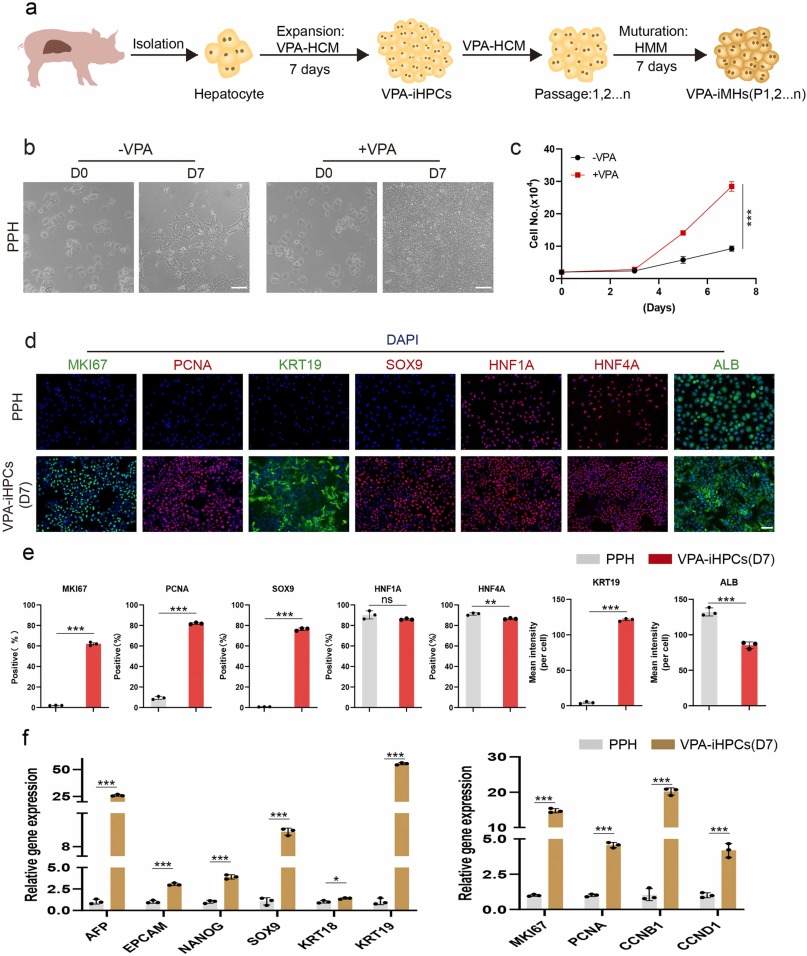
HDACi (VPA)诱导原代猪肝细胞在体外去分化为肝祖细胞(VPA-iHPCs):作者通过实验发现,原代猪肝细胞可在VPA-HCM中实现快速生长(图2c),经7天培养后,与新鲜猪肝细胞相比具有明显的肝祖细胞(VPA诱导去分化的肝祖细胞简称:VPA-iHPCs)特征,即具有更高的核质比(图2b)。免疫荧光染色结果表明,在细胞周期标志物(MKI67、PCNA)及HPC标志物(KRT19、SOX9)水平有明显提升,而与肝细胞功能相关的基因表达略(HNF1A、HNF4A和白蛋白)有降低(图2d和e)。
图2.VPA诱导原代猪肝细胞在体外转化为肝祖细胞
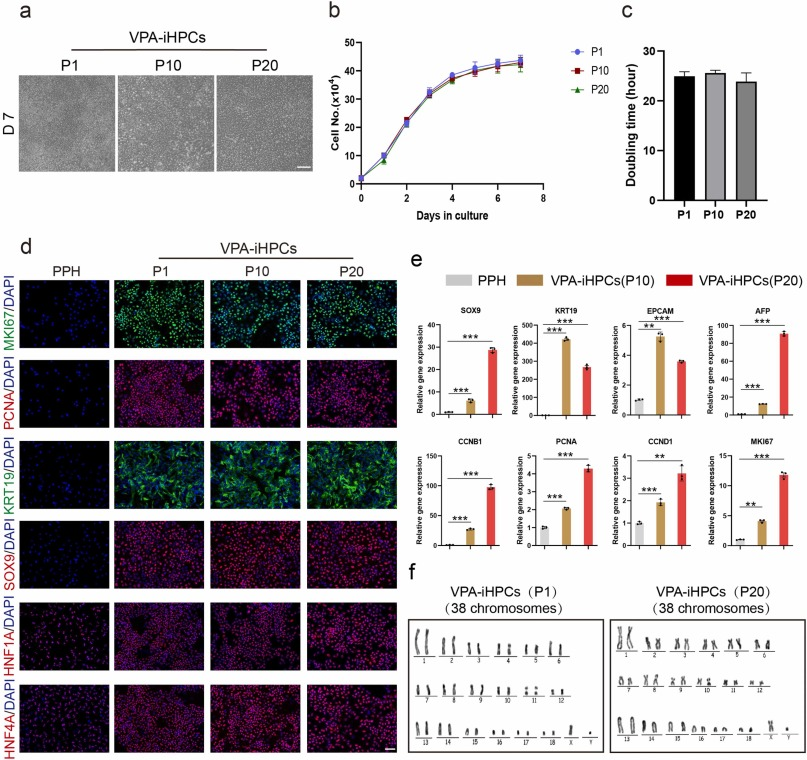
HDACi(VPA)诱导的肝祖细胞(VPA-iHPCs)在长期体外培养过程中保持其特性:培养VPA-iHPC经 6~7天传20代以上,去分化细胞仍能保持肝祖细胞的典型特征(图3b和c)。免疫荧光染色结果表明,在第1、10和20代时,VPA-iHPCs中细胞周期标记物(MKI67、PCNA)和HPC标记物(KRT19、SOX9)实现稳定高表达,而肝细胞标志物也保持了一定的表达水平(图3d和e)。
图3. VPA-iHPCs在长期体外培养过程中保持肝祖细胞特性
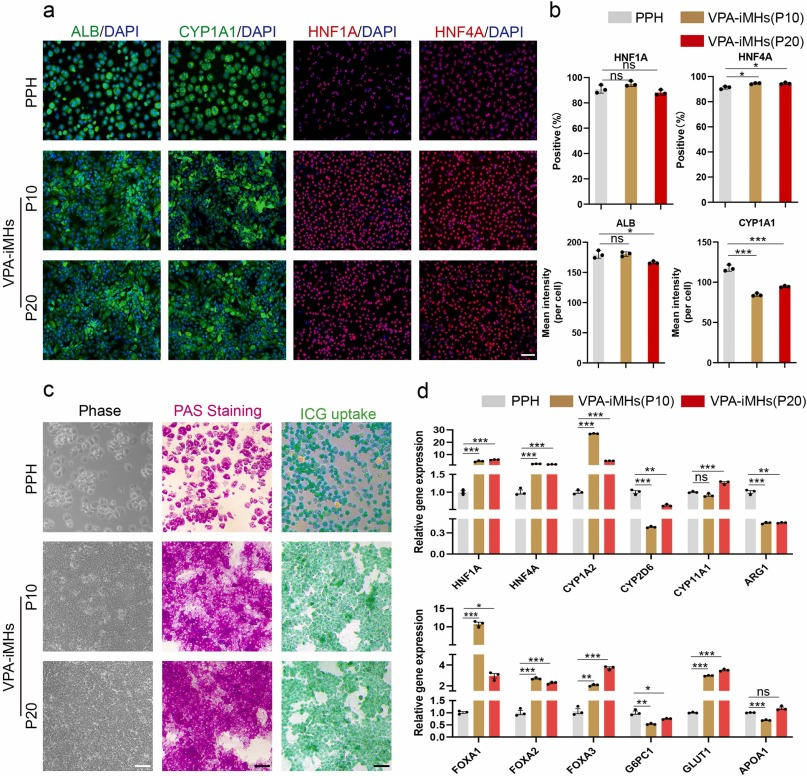
HDACi诱导的肝祖细胞(VPA-iHPCs)在体外长期培养过程中保留了分化为成熟肝细胞(VPA-iMHs)的潜力:VPA-iHPCs在常用肝细胞成熟培养基(HMM)培养7天,被成功分化出成熟肝细胞典型形态的细胞(VPA-iMHs)。免疫荧光染色结果表明,在第10和20代VPA-iMHs中成熟肝细胞相关基因表达(ALB、CYP1A1、HNF1A和HNF4A)显著增加,这一表达结果与原代肝细胞表达水平相当(图4a和b)。
图4. VPA-iHPCs 在体外长期培养过程中保留了分化为成熟肝细胞的潜力
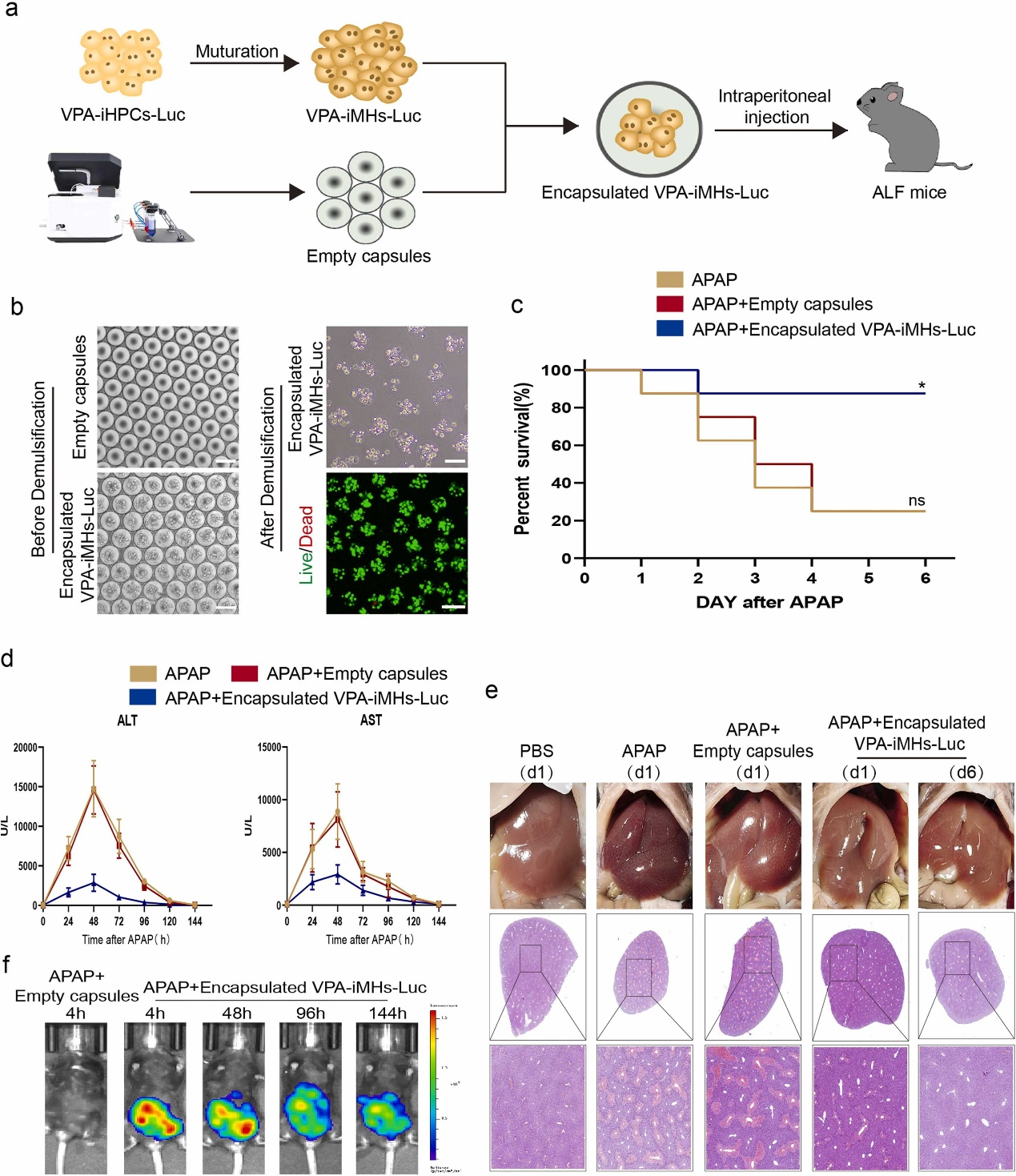
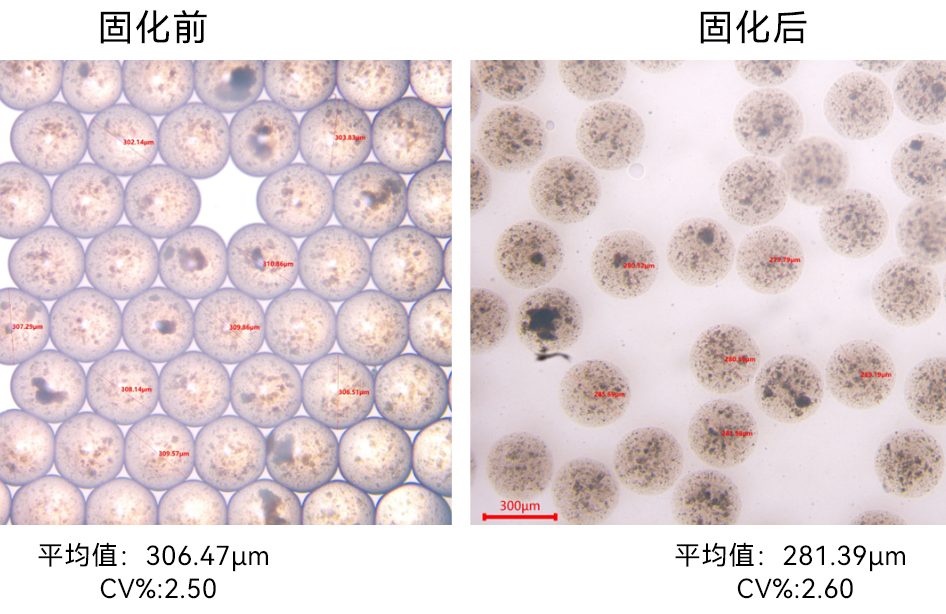
HDACi (VPA)诱导去分化再分化的成熟肝细胞(VPA-iMHs)用于治疗小鼠急性肝衰竭:作者通过微滴制备仪DG-01用海藻酸盐微球包裹VPA-iMHs使其免受宿主免疫攻击,同时能进行正常新陈代谢保持其高活性,然后将其移植到急性肝衰竭小鼠体内进行为期6天的观察和采样分析(图5a)。最终实验结果表明,相比于对照组APAP(8只小鼠存活2只),移植封装VPA-iMHs海藻酸盐的小鼠(APAP+Encapsulated VPA-iMHs-Luc)具有更高的存活率(8只小鼠存活7只)(图5c)。
图5. 使用 VPA-iMHs 治疗小鼠急性肝衰竭
【讨论与总结】
综上所述,作者通过借助HADCi(VPA)成功地将原代猪肝细胞去分化为高增殖能力的肝祖细胞(VPA-iHPCs),进而实现猪肝细胞的长期体外扩增,且保留了分化为成熟肝细胞的能力。在功能上,由HADCi(VPA)诱导去分化后再分化的成熟肝细胞(VPA-iMHs)与原生猪肝细胞表现相近,可显著提高急性肝衰竭小鼠的存活率。
【原文链接】
https://www.sciencedirect.com/science/article/pii/S0753332224008576?via%3Dihub#fig0010
| 产品图片 | 产品名称 |
 |
FluidicLab微滴/微球制备仪(DG01)
|